Polysciences PEI工业化生产实操干货,从培养基到质粒的全流程参数控制
本文摘要
本文聚焦聚乙烯亚胺(PEI)介导的细胞转染技术,基于Polysciences PEI转染试剂在AAV、慢病毒(LV)包装与重组蛋白工业化生产中的成熟应用经验,严格忠实原文数据系统拆解了影响转染效率与最终产量的5大核心关键因素,详解了培养基选择、培养体积控制、细胞质量管控、细胞密度优化、质粒质量与用量规范的实操标准与优化范围,为科研与工业化生产提供可直接落地的转染优化指南,解决转染产量参差不齐、批次稳定性差的行业痛点。
一、引言
1.1 PEI转染的核心技术原理
聚乙烯亚胺 (Polyethylenimine, PEI) 是一种水溶性阳离子高分子聚合物,其分子结构中每相隔两个碳原子就存在一个可质子化的氨基氮原子,使得聚合物网络在任何pH下都能充当有效的质子海绵体,这也是其实现高效转染的核心基础。
早在1995年,PEI就被应用于体外核酸转染,其核心作用机制分为两个关键环节:
- 核酸凝聚与复合物形成:带正电荷的PEI通过静电作用缩聚带负电的核酸,形成易被细胞摄取的正电纳米级复合体,保护核酸不被核酸酶降解;
- 内涵体逃逸与核酸释放:PEI所含的大量胺基通过质子海绵效应,促使PEI-核酸复合物逃离内涵体和溶酶体,在胞内释放核酸,最终实现目的基因的高效表达。
目前市面上的PEI转染试剂,核心原理均基于上述机制,差异主要集中在PEI的分子结构、分子量、纯度与质控标准上。
1.2 Polysciences PEI产品体系简介
Polysciences成立于1961年,其PEI转染试剂凭借稳定的转染效果,已被广泛应用于AAV、LV和重组蛋白的工业化生产,成为科研机构与生物技术公司的主流选择。其PEI产品覆盖从科研到商业化生产的全流程需求,核心产品系列如下:
| 产品名称 | 产品型号 | 规格 | 产品等级 | 质控标准 |
|---|---|---|---|---|
| PEI MAX | cat# 24765 | 1g包装 | 研究级固体粉末 | 标准QC |
| Transporter 5 | cat# 26008 | 5mL、50mL包装 | 研究级溶液 | 标准QC |
| MAXgene GMP 粉末 | cat# 26435 | 1g包装 | 商业生产级 | 严格验证QC |
| MAXgene GMP 溶液 | cat# 26406 | 1L包装 | 商业生产级 | 严格验证QC |
在工业化生产中,转染后的病毒滴度、蛋白产量是核心考核指标,但不同项目、不同操作体系下,最终产量往往参差不齐。其核心原因在于转染全流程存在多个关键影响因素,任何一个环节的参数偏差,都会导致最终结果的波动。本文将系统拆解这些关键影响因素,提供标准化的优化方向与实操规范。
二、影响PEI转染效率的5大核心因素
2.1 培养基配方:筛选适配体系,严格管控血清含量
细胞培养基是盐、碳水化合物、维生素、氨基酸、代谢前体、微量元素组成的复杂混合物,直接决定了细胞的生长状态,同时也会显著影响转染复合物的形成与转染效率。
2.1.1 培养基的筛选与推荐
不同培养基的营养成分差异,会直接影响细胞生长速率与最终的病毒/蛋白产量。如图1测试结果显示,5种不同培养基均能支持细胞指数增长,但培养基A的细胞生长状态与AAV产量显著优于其他组别,证明筛选适配的培养基是转染优化的首要环节。
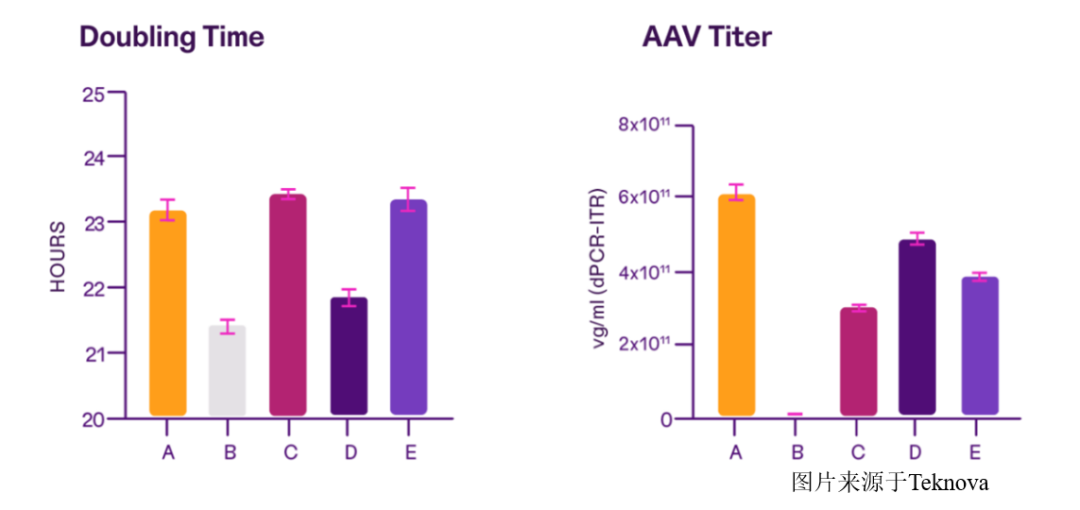
结合Polysciences PEI转染试剂的应用验证,推荐用于细胞培养与复合物稀释的培养基如下表所示:
表1 PEI转染推荐培养基清单

2.1.2 血清的管控规范
血清是包含生长因子的不确切成分添加物,其质量波动会直接影响细胞生长,同时血清中的蛋白因子会严重阻碍质粒DNA与PEI的静电结合,导致转染复合物形成失败,最终大幅降低转染效率。核心管控规范如下:
- 转染前细胞培养,推荐使用无血清或低血清(2%-5%)培养基;
- 质粒DNA与PEI孵育稀释时,必须使用无血清培养基,全程严格禁止血清添加;
- 转染前对新加入的培养基进行37℃预热,可有效降低细胞应激,提升转染效果。
2.2 培养空间:摇瓶培养体积严格控制,保障体系溶氧与营养供给
对于悬浮细胞的蛋白/病毒生产,小体积摇瓶的条件摸索是规模化放大的基础,而培养体积对最终产量的影响,是极易被忽略的关键环节。
当摇瓶内培养体积过大时,会直接导致体系内营养快速耗尽、氧气浓度不足,无法支撑细胞正常生长,造成细胞活力下降、代谢异常,最终导致转染失败、产量不达预期。
摇瓶培养体积的标准化规范:
- 摇瓶总容量<500ml时,细胞培养总体积不超过摇瓶总容量的20%,最优范围为15%-20%;
- 摇瓶总容量>500ml时,细胞培养总体积不超过摇瓶总容量的30%,最优范围为25%-30%。
2.3 细胞质量:优先选择对数生长期、低代次、高活力细胞
细胞质量是决定转染效果的核心基础,细胞的生长状态、传代次数、汇合度都会直接影响转染效率与最终产量。
2.3.1 细胞代次严格管控
细胞经过长期传代后,会发生突变、染色体重组或基因调控改变,导致生物学性状发生漂移,直接影响转染相关的细胞行为。如图2测试结果显示,相同转染参数下,低代次(p8)、中代次(p37)、高代次(p55)细胞的转染效率与稳定性存在显著差异,高代次细胞的转染结果稳定性大幅下降。
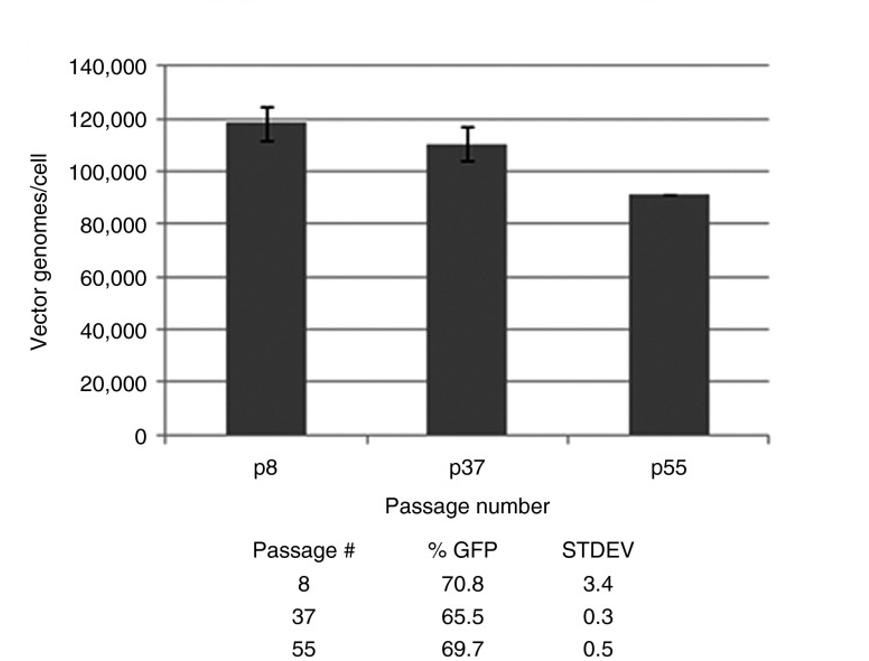
核心管控规范:
- 最适合转染的细胞,是经过几次传代后达到对数生长期的细胞,此时细胞生长旺盛、代谢活跃,转染效率最高;
- 病毒/抗体生产用细胞,传代次数最好不超过30代,低细胞代次能最大程度保障基因型稳定;
- 若发现转染效率持续下降,可复苏新的低代次细胞,恢复最佳转染效果。
2.3.2 细胞状态与汇合度要求
- 悬浮细胞:必须选用活力>95%、处于对数生长期的细胞,细胞倍增时间越短,转染效率越高;
- 贴壁细胞:转染前细胞汇合度需达到最优区间,细胞间的直接接触与旁分泌通讯,是细胞正常生长分裂的基础,汇合度过高或过低都会显著降低转染效率。
2.4 细胞密度:精准控制转染前细胞密度,适配不同培养体系
悬浮培养体系中,细胞密度直接决定了细胞的生长状态、代谢负荷与核酸摄取效率,密度过高或过低都会直接影响转染效果与产毒能力。
- 细胞密度过低:细胞间相互作用不足,易发生自发分化,细胞功能异常,转染效果与产毒能力显著下降;
- 细胞密度过高:细胞间营养与空间竞争加剧,代谢副产物(如乳酸)大量积累,细胞毒性提升,生长速率与活力下降,最终降低转染效率与产物产量。
细胞密度优化规范:
- 常规转染推荐转染前细胞密度控制在2×10^6 cells/ml左右,优化范围为1~3×10^6 cells/ml;
- 高细胞密度转染(4~5×10^6 cells/ml)可根据需求尝试,高密转染需酌情降低质粒用量,避免代谢负荷过高。
2.5 质粒DNA:严格把控质量,精准优化用量
高质量的质粒DNA是PEI转染成功的核心前提,质粒的纯度、内毒素含量、用量都会直接影响转染复合物的有效形成与最终转染效率。
2.5.1 质粒DNA的质量标准
PEI转染基于正负电荷静电吸引的原理,质粒中的蛋白、盐离子、RNA、内毒素等杂质,都会显著干扰转染复合物的形成,核心质量标准如下:
- 纯度要求:通过紫外分光光度法检测,质粒A260/A280值需在1.8~1.95之间;<1.8表明存在蛋白或酚类污染,>2.0表明存在RNA污染;
- 内毒素管控:质粒抽提过程中必须彻底清除内毒素,内毒素会引发细胞毒性,即使高浓度质粒也无法获得理想转染效果,是决定转染成败的关键指标;
- 无菌要求:质粒需无菌、无支原体污染,避免转染后体系污染导致实验失败。
2.5.2 质粒用量的优化规范
质粒用量过低会导致转染效率不足,用量过高同样会破坏转染复合物的稳定性,降低转染效率,必须通过梯度优化锁定最优用量,核心规范如下:
- 常规低细胞密度转染,初始推荐质粒用量1μg / 1×10^6 cells,优化范围为1~2μg / 1×10^6 cells;
- 高细胞密度转染(如5×10^6 cells/ml),质粒用量需同步下调,推荐用量为0.4~0.6μg / 1×10^6 cells,避免细胞代谢负荷过高。
三、后续优化方向预告
除本文详解的5大核心因素外,质粒配比、PEI与DNA的比例、复合物孵育时间、病毒/蛋白收获时间等因素,同样会对最终生产产量产生显著影响。完整的转染工艺优化,需对全流程参数进行系统性的梯度测试与锁定。
更多转染优化的核心细节与实操规范,可关注后续《细胞转染优化方向(二)》的完整内容。
四、FAQ 高频技术问题解答
1. 问:PEI转染时,推荐使用哪些培养基?复合物稀释液有什么核心要求?
答:细胞培养推荐使用Hycell TransFx-H、Ex-Cell 293无血清培养基、Freestyle 293表达培养基、ESF无血清培养基;复合物稀释推荐使用Opti-MEMTM、OptiPROTM SFM、无血清Freestyle 293培养基,核心要求是稀释液必须无血清,血清中的蛋白会阻碍质粒与PEI的结合,导致转染效率下降。
2. 问:HEK293悬浮细胞摇瓶培养时,推荐的培养体积占比是多少?为什么?
答:摇瓶总容量<500ml时,培养体积不超过总容量的20%;总容量>500ml时,培养体积不超过总容量的30%。核心原因是体积过大会导致摇瓶体系内溶氧不足、营养快速耗尽,造成细胞生长状态异常,最终降低转染效率与产物产量。
3. 问:用于PEI转染的细胞,代次控制在多少以内合适?高代次细胞会有什么影响?
答:推荐使用30代以内的低代次细胞进行转染。细胞经过长期高代次传代后,会发生基因突变、染色体重组或基因调控改变,生物学性状发生漂移,导致转染效率下降、批次稳定性变差,甚至影响最终的病毒/蛋白表达效果。
4. 问:PEI转染的推荐细胞密度是多少?高细胞密度转染时要注意什么?
答:常规转染推荐细胞密度为1~3×10^6 cells/ml,最优初始值为2×10^6 cells/ml;高细胞密度转染(4~5×10^6 cells/ml)时,必须酌情降低质粒用量,推荐0.4~0.6μg / 1×10^6 cells,避免细胞代谢负荷过高、毒性副产物积累,导致细胞活力下降。
5. 问:用于PEI转染的质粒DNA有什么核心质量要求?推荐用量是多少?
答:质粒核心质量要求:A260/A280值在1.8~1.95之间,无蛋白、RNA污染,内毒素彻底清除,无菌无支原体。常规转染初始推荐质粒用量为1μg / 1×10^6 cells,优化范围1~2μg / 1×10^6 cells;高密转染需下调至0.4~0.6μg / 1×10^6 cells。
6. 问:转染复合物制备时,为什么要严格限制血清的使用?
答:PEI与质粒DNA的结合依赖正负电荷的静电作用,而血清中存在大量蛋白因子,会与PEI竞争结合质粒DNA,直接破坏转染复合物的形成,导致复合物无法被细胞有效摄取,最终大幅降低转染效率,因此复合物稀释孵育全程必须使用无血清培养基。
五、总结
PEI转染的最终效果,并非由单一参数决定,而是依赖全流程多个关键因素的协同优化。本文详解的培养基筛选、培养体积控制、细胞质量管控、细胞密度优化、质粒质量与用量规范,是转染工艺优化的基础核心环节。
在AAV、慢病毒包装与重组蛋白的工业化生产中,只有对上述参数进行系统性的梯度测试、标准化锁定,才能最大程度保障转染效率的稳定性,实现产物产量的批次可控,解决转染结果参差不齐的核心痛点。
六、参考文献
[1] Cell culture media for recombinant protein expression in Chinese hamster ovary (CHO) cells: History, key components, and optimization strategies.
[2] Production of Recombinant Adeno-associated Virus Vectors Using Suspension HEK293 Cells and Continuous Harvest of Vector From the Culture Media for GMP FIX and FLT1 Clinical Vector.
[3] Comparison of highly pure rAAV9 vector stocks produced in suspension by PEI transfection or HSV infection reveals striking quantitative and qualitative differences.
[4] A feasibility study of different commercially available serum‑free mediums to enhance lentivirus and adeno‑associated virus production in HEK293 suspension cells.
[5] Adeno-Associated Virus Production, Purification, and Titering.
[6] Non-Viral in Vitro Gene Delivery: It is Now Time to Set the Bar!
[7] Polyethylenimine (PEI) in gene therapy: Current status and clinical applications.
[8] Protocol for Efficient Generation and Characterization of Adeno-Associated Viral Vectors.
[9] Lentiviral Vector Production in Suspension Culture Using Serum-Free Medium for the Transduction of CAR-T Cells.
[10] Development of a scalable process for high-yield lentiviral vector production by transient transfection of HEK293 suspension.
技术来源说明
本文内容整理自原文技术资料,上海曼博生物医药科技有限公司为Polysciences品牌Kyfora PEI转染试剂官方授权供应商,专注于为细胞治疗、基因治疗领域提供合规的转染试剂与技术解决方案。
