Sexton PR hPL对比FBS/人AB血清的T细胞培养性能实验数据全拆解
本文摘要
本文聚焦CAR-T细胞治疗工业化生产的核心痛点——T细胞体外培养的合规性、转导效率与细胞质量控制,基于多供体平行实验数据,系统解析了病原体减少工艺人血小板裂解液(PR hPL)作为无动物源血清替代物,在人T细胞体外慢病毒转导、扩增、亚群比例维持与分化表型调控中的综合性能表现。文中通过4组核心对比实验,验证了hPL与传统胎牛血清(FBS)、人AB血清的性能差异,证实hPL可实现与AB血清相当的慢病毒转导效率与T细胞扩增倍数,同时有效维持CD4/CD8细胞亚群的生理比例,显著提升初始T细胞(TN)与中央记忆T细胞(TCM)低分化表型占比,为CAR-T等免疫细胞治疗产品的体外培养提供了合规、高效、稳定的无动物源解决方案,完全符合国内《细胞治疗产品研究与评价技术指导原则(试行)》的监管要求。
一、引言
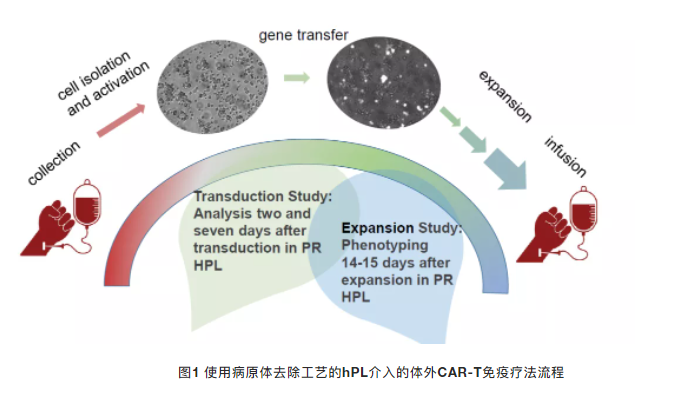
CAR-T细胞治疗作为突破性的肿瘤免疫治疗技术,已在血液肿瘤领域实现了显著的临床疗效。其标准化生产流程通常为:通过白细胞分离技术从患者或健康供体采集外周血单个核细胞,完成T细胞富集后,通过病毒载体进行基因修饰,最终经体外扩增获得足量的CAR-T细胞成品。
而T细胞的体外培养与扩增,是CAR-T生产的核心环节,同时也是监管核查的重点。国家药品监督管理局发布的《细胞治疗产品研究与评价技术指导原则(试行)》中明确指出:细胞培养过程中,应尽量避免使用动物来源的物质,若必须使用血清,需提供使用必要性与合理性的研究资料;严禁使用疫病流行区来源的动物血清,不得使用未经过安全性验证的血清。
传统CAR-T细胞培养体系中常用的FBS存在明确的动物源合规风险,人AB血清则存在供体依赖、批次差异大、供应不稳定等问题。因此,开发安全、成分明确、性能稳定的无动物源血清替代物,已成为细胞治疗行业工业化发展的核心需求。
本文基于完整的多供体对比实验,系统解析了美国Sexton品牌PR工艺hPL作为血清替代物,在T细胞体外转导、扩增、表型维持全流程中的性能表现,为CAR-T细胞治疗的工艺优化与合规化生产提供完整的实验依据。
二、实验材料与方法
2.1 实验材料
- 细胞样本:健康供体来源的人外周血T细胞;
- 培养基补充剂:美国Sexton品牌病原体减少工艺hPL(PR hPL)、人AB血清、胎牛血清FBS;
- 主要试剂:CD3/CD28 T细胞激活剂、IL-2、CMV-GFP慢病毒颗粒、流式细胞术检测抗体(抗CD4、CD8、CD45RO、CCR7、CD127、CD62L抗体);
- 主要设备:血细胞计数仪、流式细胞仪、荧光显微镜。
2.2 实验方法
- T细胞处理:按照标准流程完成人外周血T细胞的解冻、复苏,使用CD3/CD28 T细胞激活剂完成T细胞激活;
- 分组培养:将激活后的T细胞,分别接种于添加5% PR hPL、5%人AB血清、5% FBS的培养基中(均含等量IL-2),于12孔板中进行平行培养;
- 慢病毒转导:T细胞解冻激活4天后,使用CMV-GFP慢病毒颗粒进行体外转导,分别于转导后2天、7天完成转导效率检测;
- 扩增性能检测:培养周期内定时通过血细胞计数仪完成细胞计数,绘制细胞生长曲线,统计总扩增倍数;
- 流式表型分析:通过免疫荧光染色与流式细胞术,完成T细胞亚群(CD4/CD8)、分化相关标志物(CD45RO、CCR7、CD62L)的检测,分析T细胞分化表型。
三、核心实验结果与分析
3.1 实验一:hPL对慢病毒转导T细胞效率的影响
本实验核心验证hPL作为培养基补充剂,是否会影响慢病毒对T细胞的转导效率,分别在转导后2天、7天检测GFP阳性细胞比例,同时检测转导7天后的平均荧光强度,评估转基因表达水平。
3.1.1 实验设计
- 分组设置:5%人AB血清组、5% PR hPL组;
- 检测节点:转导后2天(转导直接影响最小时间点)、转导后7天(间接影响显现时间点);
- 检测指标:GFP阳性细胞百分比、平均荧光强度;
- 样本量:4名独立健康供体,每组设置3个重复孔。
3.1.2 核心实验结果
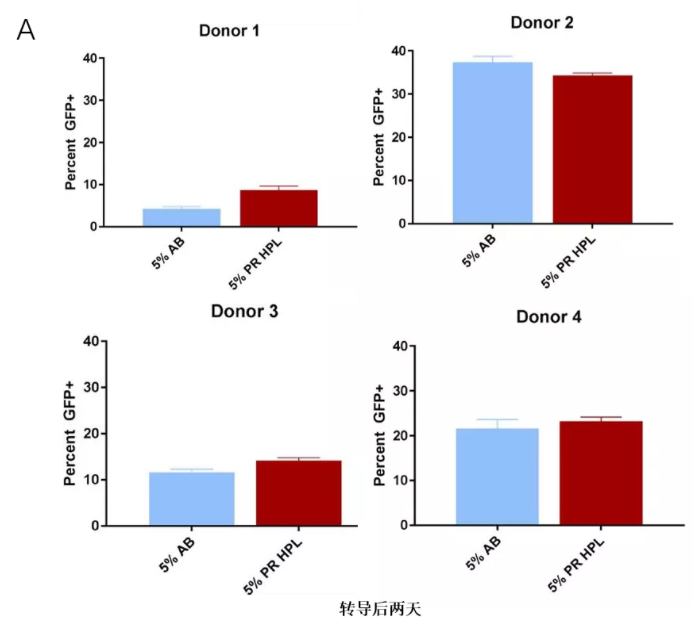
- 转导后2天:4名供体的平行实验均显示,5% PR hPL组与5%人AB血清组的GFP阳性细胞百分比无显著差异,二者慢病毒转导效率相当;
- 转导后7天:两组的GFP阳性细胞百分比仍无统计学差异,证实hPL不会因长期培养影响转导阳性细胞的存活与增殖;
- 平均荧光强度:转导7天后,两组的平均荧光强度无显著差异,证实hPL培养体系中,T细胞的转基因表达水平与AB血清组相当,甚至部分供体呈现更稳定的转基因表达趋势。
核心结论:在5%使用浓度下,PR hPL作为T细胞培养补充剂,可实现与人AB血清相似的慢病毒转导效率,不会对慢病毒介导的T细胞基因修饰产生负面影响。
3.2 实验二:hPL对T细胞扩增效率的影响
细胞扩增效率直接决定CAR-T生产的最终收率,是工业化生产的核心指标。本实验对比了不同培养基补充剂对T细胞体外扩增能力的影响。
3.2.1 实验设计
- 分组设置:5% FBS组、5%人AB血清组、5% PR hPL组、基础培养基对照组;
- 培养周期:13-14天,培养周期内定时完成细胞计数;
- 检测指标:细胞生长曲线、培养终点总扩增倍数;
- 样本量:4名独立健康供体。
3.2.2 核心实验结果
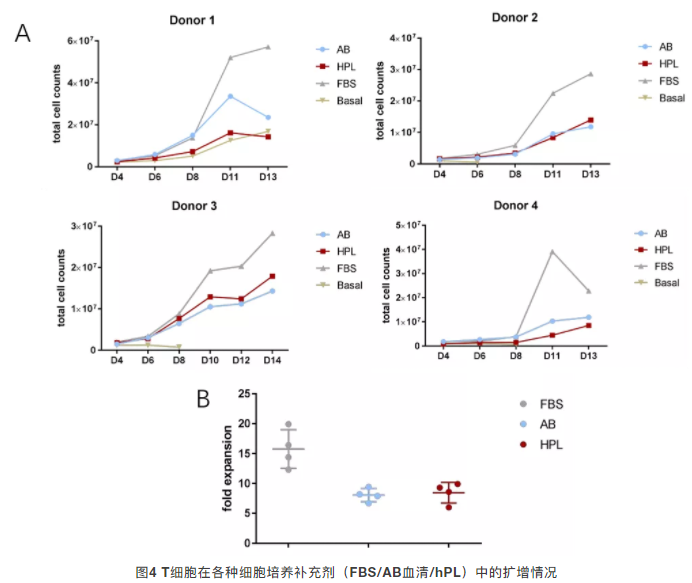
- 生长曲线:整个培养周期内,PR hPL组的T细胞生长趋势与人AB血清组、FBS组高度一致,无增殖延迟或抑制现象;
- 总扩增倍数:培养终点(第13-14天)的统计结果显示,5% PR hPL组的T细胞总扩增倍数,与人AB血清组无统计学差异,二者均显著优于基础培养基对照组;
- 供体一致性:4名供体的实验结果呈现高度一致的趋势,证实hPL对不同供体来源的T细胞均具备稳定的扩增支持能力。
核心结论:在5%使用浓度下,PR hPL作为T细胞培养补充剂,可实现与人AB血清、FBS相当的T细胞扩增效率,完全满足CAR-T细胞规模化生产的扩增需求。
3.3 实验三:hPL对T细胞CD4/CD8亚群比例的影响
CD4+辅助性T细胞与CD8+细胞毒性T细胞的比例,是CAR-T细胞成品质量控制的关键指标,生理状态下的CD4/CD8比例(40/60-60/40)对CAR-T细胞的体内疗效与持久性至关重要。
3.3.1 实验设计
- 分组设置:5%人AB血清组、5% PR hPL组;
- 检测节点:培养扩增14天后;
- 检测指标:CD4+、CD8+ T细胞亚群占比,CD4/CD8比值;
- 样本量:4名独立健康供体,每组设置3个重复孔。
3.3.2 核心实验结果
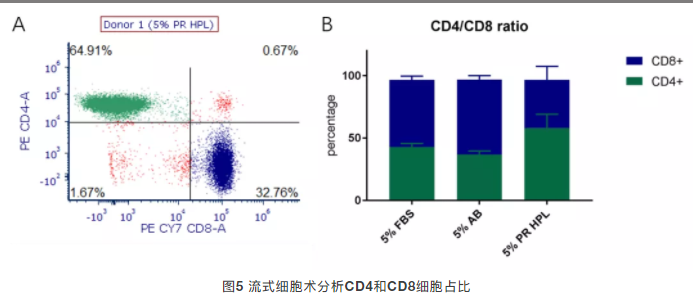
- 流式细胞术分析结果显示,5% PR hPL组培养的T细胞,CD4/CD8比值稳定维持在40/60-60/40的生理范围内;
- 与人AB血清组相比,PR hPL组可更好地维持T细胞CD4/CD8亚群的生理比例,避免亚群失衡。
核心结论:PR hPL作为T细胞培养补充剂,有助于维持T细胞CD4/CD8亚群的生理比例,保障CAR-T细胞成品的表型均一性与质量稳定性。
3.4 实验四:hPL对T细胞低分化水平的维持作用
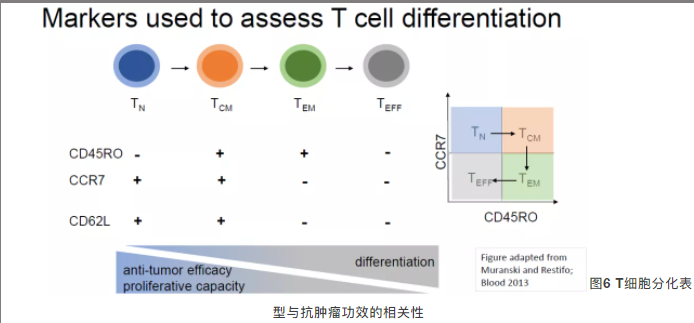
已有大量研究证实,低分化的初始T细胞(TN)与中央记忆T细胞(TCM),具备更强的体内扩增能力、持久性与长期抗肿瘤疗效,是决定CAR-T细胞治疗长期临床获益的关键因素。本实验核心验证hPL对T细胞分化表型的调控作用。
3.4.1 实验设计
- 分组设置:5% FBS组、5%人AB血清组、5% PR hPL组;
- 检测节点:培养扩增14-15天后;
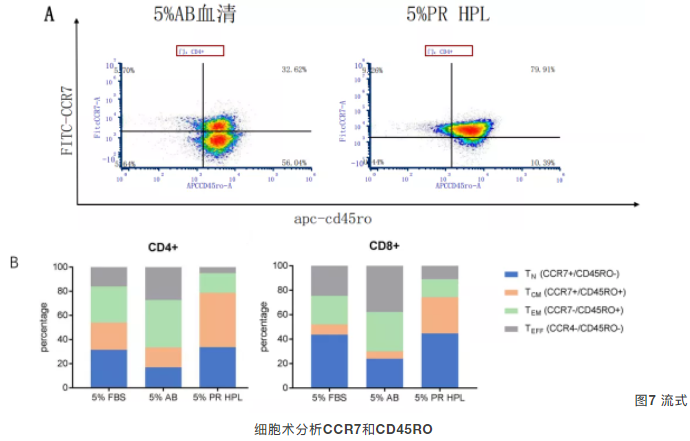
- 检测标志物:T细胞分化核心标志物CD45RO、CCR7、CD62L,通过流式细胞术区分TN(CCR7+/CD45RO-)、TCM(CCR7+/CD45RO+)、TEM(CCR7-/CD45RO+)、TEFF(CCR7-/CD45RO-)细胞亚群占比;
- 样本量:3-4名独立健康供体。
3.4.2 核心实验结果
- 分化亚群占比:与人AB血清组相比,PR hPL组培养的CD4+、CD8+ T细胞中,终末分化的TEM/TEFF(CCR7-)细胞占比显著降低,而TN、TCM低分化亚群占比显著提升,其中TCM细胞占比达到AB血清组的3-5倍,4名供体均呈现一致的表型变化趋势;
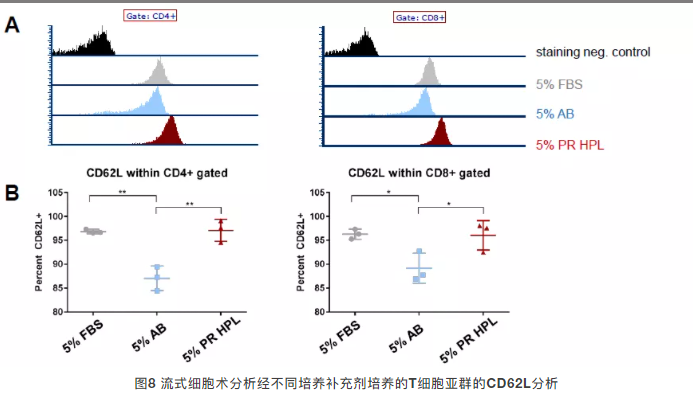
- CD62L表达:CD62L是T细胞归巢与记忆特性的核心标志物,实验结果显示,PR hPL组的CD4+、CD8+ T细胞中,CD62L+细胞占比显著高于FBS组与人AB血清组,差异具备统计学意义(p<0.05);
- 综合表型:hPL培养体系可有效抑制T细胞在体外扩增过程中的终末分化,支持T细胞维持更低的分化水平,保留更强的体内持久性与抗肿瘤潜能。
核心结论:PR hPL作为T细胞培养补充剂,可有效支持T细胞维持低分化水平,显著提升TN/TCM细胞亚群占比,为CAR-T细胞赋予更优的体内长期抗肿瘤能力。
四、综合研究结论
通过4组系统性的多供体对比实验,可得出三大核心结论,为CAR-T细胞治疗的培养基体系优化提供明确的实验依据:
- 性能等效性:PR hPL作为FBS、人AB血清的替代物,用于T细胞体外培养时,可实现与人AB血清相当的慢病毒转导效率与T细胞扩增倍数,完全满足CAR-T生产的核心工艺需求;
- 质量提升性:PR hPL可有效维持T细胞CD4/CD8亚群的生理比例,同时显著提升TN/TCM低分化表型占比,TCM占比可达AB血清组的3-5倍,有效抑制T细胞体外扩增过程中的终末分化,显著提升CAR-T细胞成品的质量与体内抗肿瘤潜能;
- 合规适配性:PR hPL作为无动物源的人源化培养基补充剂,完美规避了FBS的动物源监管风险,同时具备优异的批次稳定性,符合国内《细胞治疗产品研究与评价技术指导原则(试行)》的相关要求,适配CAR-T细胞治疗产品从研发到临床申报、商业化生产的全流程需求。
此外,实验中还观察到,hPL培养体系中的T细胞呈现更稳定的转基因表达水平,意味着在实现相同转导效果的前提下,可减少慢病毒的使用量,进一步降低CAR-T产品的生产成本与工艺风险。综上,Sexton PR hPL是CAR-T细胞治疗中T细胞体外培养的理想无动物源血清替代物。
五、FAQ 高频技术问题解答
1. 问:hPL作为培养基补充剂,会影响慢病毒对T细胞的转导效率吗?
答:不会。多供体平行实验证实,5%浓度的PR hPL培养体系,可实现与人AB血清相当的慢病毒转导效率,无论是转导后2天的早期转导阳性率,还是转导后7天的长期阳性率、转基因平均荧光强度,均与AB血清组无显著差异,不会对慢病毒介导的T细胞基因修饰产生负面影响。
2. 问:hPL相比人AB血清,在T细胞扩增上有什么优势?
答:在扩增效率上,hPL可实现与人AB血清相当的T细胞总扩增倍数,完全满足CAR-T生产的收率需求;除此之外,hPL具备三大核心优势:一是批次稳定性更优,通过多供体混合生产最大限度降低批间差异,规避了AB血清的供体依赖问题;二是可有效维持T细胞CD4/CD8亚群的生理比例,保障细胞成品的表型均一性;三是可显著提升TN/TCM低分化表型占比,赋予CAR-T细胞更强的体内持久性与抗肿瘤疗效。
3. 问:为什么hPL能维持T细胞的低分化表型?这种表型对CAR-T治疗有什么意义?
答:hPL中含有丰富的血小板来源生长因子、细胞因子与趋化因子,可协同调控T细胞的分化进程,抑制体外扩增过程中的终末分化,从而维持TN/TCM低分化表型。这种低分化表型对CAR-T治疗意义重大:已有大量临床前与临床研究证实,TN/TCM亚群的CAR-T细胞,具备更强的体内扩增能力、更长的体内持久性与更优异的长期抗肿瘤疗效,直接决定了CAR-T治疗的长期临床获益,同时可有效降低肿瘤复发风险。
4. 问:hPL培养体系,是否符合国内细胞治疗产品的监管要求?
答:完全符合。国内《细胞治疗产品研究与评价技术指导原则(试行)》明确要求,细胞培养过程中应尽量避免使用动物来源的物质。hPL为人源化的无动物源培养基补充剂,完全规避了FBS的动物源伦理与安全风险;同时Sexton PR hPL在ISO9001认证设施中生产,完成了病原体减少工艺验证,通过了无菌、支原体、内毒素等全套质控检测,已在FDA备案生物制品主文件(BMF),具备完整的合规性支撑文件,完全适配细胞治疗产品的研发、临床申报与商业化生产需求。
5. 问:hPL用于CAR-T细胞培养,推荐的使用浓度是多少?
答:本次实验中采用的5%浓度,即可实现与人AB血清相当的转导效率与扩增效果,同时实现优异的表型维持能力。实际应用中,可根据不同的CAR结构、T细胞供体来源、培养体系与工艺需求,在2%-10%的浓度范围内进行梯度优化,锁定适配自身体系的最优使用浓度。
6. 问:hPL可以用于CAR-T之外的其他免疫细胞培养吗?
答:可以。hPL作为广谱的无动物源血清替代物,除了CAR-T细胞外,还可完美适配TCR-T、NK、CAR-NK、TIL等多种免疫细胞的体外培养与扩增,同时在间充质干细胞、内皮细胞等多种细胞的培养中也有广泛应用,是细胞治疗领域通用型的高性能血清替代物。
六、参考文献
[1] 国家药品监督管理局. 细胞治疗产品研究与评价技术指导原则(试行). 2017年第216号通告.
[2] Muranski P, Restifo NP. Essentials of T cell differentiation for adoptive cancer therapy. Blood. 2013.
[3] Hinrichs CS, et al. Type 17 effector CD8+ T cells mediate superior antitumor immunity. Proc Natl Acad Sci USA. 2009.
[4] Klebanoff CA, et al. Central memory self/tumor-reactive CD8+ T cells confer superior antitumor immunity compared with effector memory T cells. J Clin Invest. 2008.
技术来源说明
本文内容基于美国Sexton Biotechnologies官方实验数据整理,核心实验结果均来自原文多供体验证数据,无商业营销导向,仅供细胞治疗、免疫细胞培养领域的技术交流参考。
文中提及的美国Sexton品牌nLiven PR,是专为T细胞培养开发的临床级血小板裂解液产品,具备以下核心特点:可完美替代FBS与人AB血清,实现相当的T细胞转导效率与扩增倍数;采用病原体减少工艺,在ISO9001认证设施中生产,完成全套无菌、支原体、内毒素检测;通过100多名AABB认证/FDA注册血液中心健康供体的血小板混合生产,最大限度降低批间差异;符合欧洲药典相关要求,已在FDA备案生物制品主文件(BMF),全球数百个临床项目正在使用。
上海曼博生物医药科技有限公司为美国Sexton Biotechnologies品牌人血小板裂解液中国大陆地区官方授权供应商,可为细胞治疗企业提供从研发到临床级的hPL产品与全流程技术支持。
